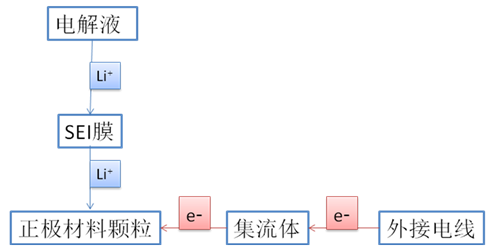
我們以磷酸鐵鋰的陽極為微系統,對系統進行分析,如圖1所示:

電池放電時,鋰離子通過電解液從負極遷移到正極材料表面的SEI膜上,再通過SEI膜進入正極顆粒;另一方面,電子通過外部連接路徑流入陰極材料顆粒,通過集電器的傳導,在陰極材料顆粒中完成還原反應。可以看出,以磷酸鐵鋰為正極材料的電池的倍率性能取決于鋰離子和電子在整個過程中的傳輸速度。查看系統的五個組件:
(1)電解液:電解液中鋰離子電導率的數量級為10-3s/cm;
(2) SEI膜:磷酸鐵鋰用電解液形成的SEI膜薄而穩定,SEI膜的孔徑大小使得鋰離子通過的影響可以忽略不計;
(3)正極材料磷酸鐵鋰:電子電導率為10-9 S/cm,鋰離子擴散速率為10-14 ~ 10-11 cm2/S;
(4)集流體為鋁箔,是電子的良導體,其對速度的影響忽略不計;
(5)外部導線是電子的良導體,對速度的影響可以忽略不計。
根據系統中各組成部分的分析,速度控制步驟是整個過程中最慢的部分,即磷酸鐵鋰材料的離子電導率和電子電導率過低。因此,有必要提高材料的電子電導率和離子電導率。我們通過物理場來分析磷酸鐵鋰這個組件在系統中的作用,如圖2所示:

磷酸鐵鋰材料傳輸電子的能力不足。利用標準解決方案的思想,我們可以引入第三方來幫助他們加強運輸功能。因此,第一個研究思路是在磷酸鐵鋰材料中加入優良的導電劑來增強正極活性材料,例如加入石墨烯、碳納米管等導電劑可以有效提高電池的倍率性能。
然后,我們利用三軸分析中的因果軸方法分析了磷酸鐵鋰材料的離子電導率和電子電導率的根本原因。首先我們必須了解磷酸鐵鋰/的晶體結構,如圖3所示:

圖3中的磷酸鐵鋰中的氧原子排列成六邊形緊密堆積,鐵和鋰原子被分成八面體中心,氧原子堆積在八面體中心。而磷原子占據氧原子四面體的4c位置。另一方面,在bc平面上,FeO6的每兩個八面體共享一個O原子。同時,每個FeO6八面體分別與兩個LiO6八面體共面,而每個PO4基團分別與FeO6八面體和LiO6八面體有一條和兩條公共邊。
磷酸鐵鋰中FeO6八面體和LiO6八面體之間的四面體PO4限制了鋰離子在充放電過程中的插入和取出,這是離子電導率低的根本原因。同時,電子傳導只能通過共價鍵Fe-O-Fe進行,這是磷酸鐵電子電導率低的根本原因。因此,磷酸鐵鋰本身的結構特點是其在充放電過程中充放電倍率性能不佳的本質原因。然而,正是因為磷酸鐵鋰的特殊結構,使其具有了其他正極材料所不具備的一系列優異性能。例如,鋰和氧之間的共價鍵結構使這種材料在高溫下很難釋放氧,這使其熱力學穩定。
通過對磷酸鐵鋰材料子系統中的四個原子:Li、O、P、Fe的分析,可以看出磷酸鐵鋰材料的缺陷和優勢來自于它的NaSICON結構。這是一組物理矛盾。在解決這個矛盾的同時,需要保留這種結構帶來的優勢,改善這種矛盾帶來的劣勢。尋求通過創新解決矛盾的思路原理;
(1)保留磷酸鐵鋰 material的結構,即保留其所有優點。同時,采用創新原理中和的思路,使原有的微米級粒子納米化。納米顆粒有效縮短了鋰離子在材料中擴散所需的路徑,減少了擴散所需的時間,從而提高了倍率性能。
(2)借助超級系統的組件改進磷酸鐵鋰系統,而不改變磷酸鐵鋰的結構。磷酸鐵鋰本身導電性差,所以我們給磷酸鐵鋰顆粒涂上一些斷電性能好的物質,幫助它們導電。
(3)保留磷酸鐵鋰材料的NaSICON結構,加入一些其他元素取代原來的原子位置,從而提高晶體的無序程度,產生有利于電子和離子傳導的缺陷,從而提高電學性能。
目前,關于優化磷酸鐵鋰的報告可以按照上述思路分為三類:
(a)研究用于改善晶粒尺寸和納米化的材料。如劉等合成的納米磷酸鐵鋰/碳材料,在80℃下可滿足95 mAh/g的放電速率。
(b)材料表面涂有導電性良好的碳或金屬離子。例如,水熱合成法在磷酸鐵鋰顆粒表面包覆導電性能良好的石墨烯時,在10°C速率下的比容量可達110 mAh/g,涂層形貌如圖4所示:

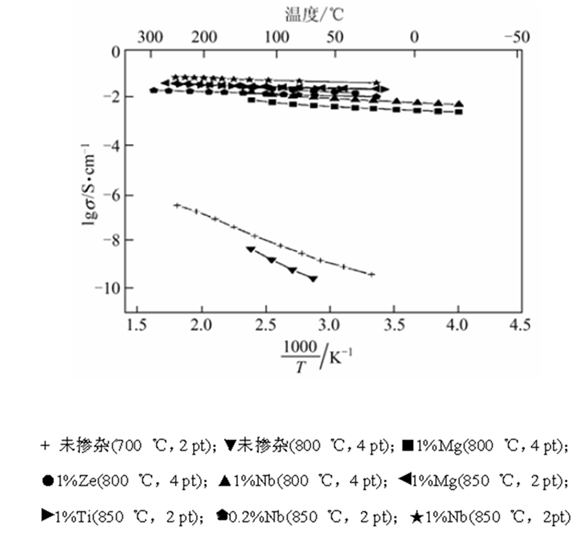
(c)金屬離子摻雜。如Chung等采用了高價金屬離子(Nb5+、Ti4+、W6+等)摻雜鋰離子的位置。)在磷酸鐵鋰晶格中,使磷酸鐵鋰和磷酸鐵鋰+晶格中的鐵原子以混合價的形式存在。如圖5所示,材料的電子電導率大大提高,從而提高了電池的倍率性能,在21.5°c的倍率下,比容量超過60 mAh/g。
粗略估計,關于磷酸鐵鋰正極材料的研究報告數量已經達到104個數量級,具體內容可以概括為TRIZ理論分析磷酸鐵鋰材料結構分析、電子電導率和離子電導率的計算、電導率改性的實驗和理論研究三個方向。經過人們的不懈努力,磷酸鐵鋰的電池體系能量密度和主要技術指標已接近其理論值,是我國主要鋰電池企業開發電動汽車用電池材料的主要電池材料。
基于氟化石墨材料的高比能量原電池中的氟化石墨材料和磷酸鐵鋰材料也面臨類似的問題。它們也是具有低電子電導率和離子電導率的相變反應材料。通過TRIZ,可以得到優化氟化石墨材料的思路和方案。